金沢大学医薬保健研究域医学系神経解剖学の宝田美佳准教授、堀修教授、大学院医薬保健学総合研究科医学専攻/ナノ精密医学・理工学卓越大学院プログラム履修者の範啓琰(博士課程 4 年)を中心とする研究グループは、脳外傷後に血管のストレス応答が働くことで、病態悪化に関わる神経炎症や脳のバリア機能破綻を抑え、脳を守る新たな仕組みを明らかにしました。
外傷性脳損傷は、交通事故や転倒、スポーツ外傷などによって起こり、若者から高齢者まで幅広い世代で問題となっている重大な疾患です。外傷直後に起こる一次障害に加えて、その後数日から数週間にわたって、炎症や脳のむくみ、神経細胞死などの二次障害が進行します。これらの二次障害は、長期にわたる後遺症の大きな原因となるため、病態の悪化を制御できる仕組みを解明し、新しい治療法を開発することが望まれています。
本研究では、同研究グループが近年見出した知見に基づき、外傷性脳損傷後の血管内皮細胞(※1)における小胞体ストレス応答(※2)に着目しました。血管内皮細胞において小胞体ストレスセンサーである IRE1 が適切に機能しないようにしたマウスでは、脳外傷後に、脳のバリア機能の破綻、免疫細胞の過剰な浸潤と神経炎症、神経障害がいずれも悪化し、結果として運動機能の回復が損なわれることが明らかになりました。さらに、小胞体ストレスを軽減する薬剤を投与すると、脳外傷モデルマウスにおいて神経症状が改善することも示されました。
本成果は、外傷性脳損傷における病態進行の理解を深めるものであり、将来的には、新しい治療法の開発に活用されることが期待されます。
本研究成果は,2026 年 2 月 9 日に英国科学誌『Cell Death & Disease』のオンライン版に掲載されました。

図1. 小胞体ストレスと小胞体ストレス応答の概要
細胞へのさまざまなストレスは、不良タンパク質の小胞体への蓄積(小胞体ストレス)を引き起こす。このような状況に対応するためのタンパク質の品質管理機構が、「小胞体ストレス応答」である。本研究では小胞体ストレスセンサーの一つ、IRE1に着目した。
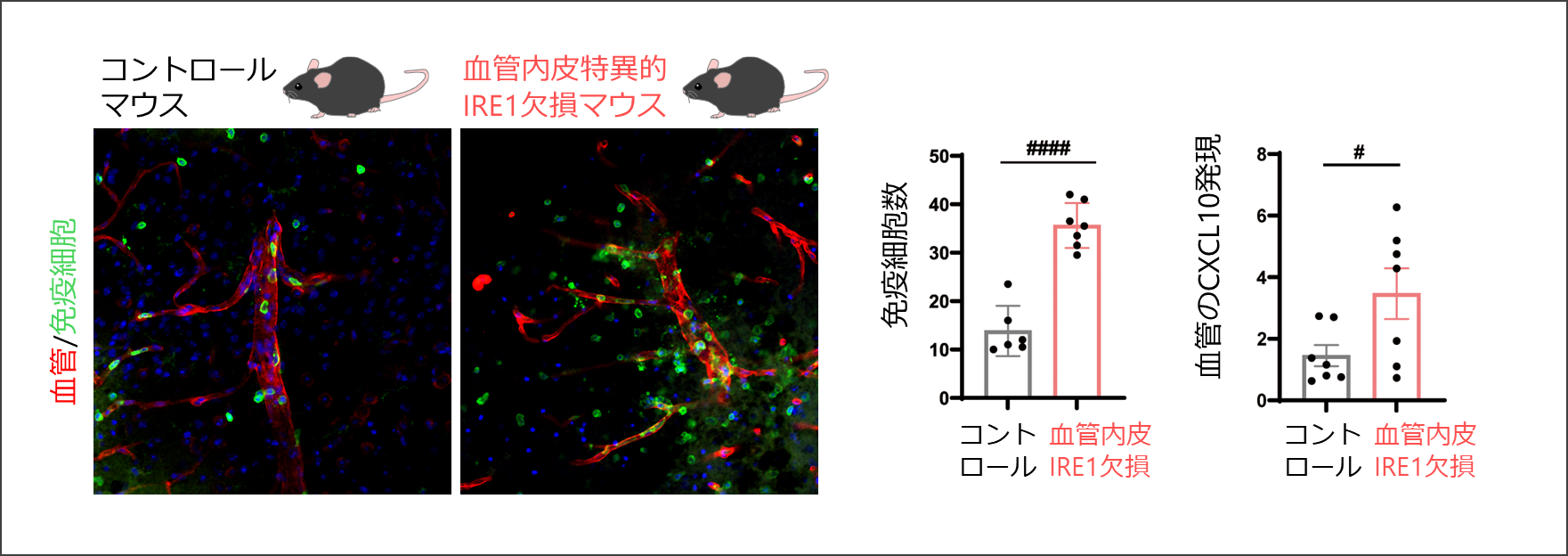
図2. 脳外傷後の免疫細胞の脳内浸潤
血管内皮特異的IRE1欠損マウスでは、脳外傷後に脳内に浸潤したCD45陽性免疫細胞数や、免疫細胞を遊走させるケモカインCXCL10の血管内皮における発現が増加した。
【用語解説】
※1 血管内皮細胞
血管の内壁をつくる細胞で、血液脳関門のバリア機能の維持に最も重要な細胞。
※2 小胞体ストレスと小胞体ストレス応答(unfolded protein response: UPR)
タンパク質を折りたたむ小胞体が過負荷に陥ると「小胞体ストレス」が生じ、細胞はそれに対処するために「小胞体ストレス応答」を誘導する。IRE1 は小胞体ストレス応答の主要な経路の一つ。
ジャーナル名:Cell Death & Disease
関連情報
金沢大学 医薬保健学域 医学類 / 大学院医薬保健学総合研究科 医学専攻:https://www.med.kanazawa-u.ac.jp/
金沢大学医薬保健研究域医学系 神経解剖学 堀研究室:https://med03.w3.kanazawa-u.ac.jp/index.html







 PAGE TOP
PAGE TOP