–
金沢大学ナノ生命科学研究所(WPI-NanoLSI)の市川壮彦特任助教、河野洋平研究員、志見剛特任准教授、福間剛士教授、がん進展制御研究所の平田英周教授らの共同研究グループは、原子間力顕微鏡(AFM)(※1)を基盤として独自に開発したナノ内視鏡原子間力顕微鏡(ナノ内視鏡 AFM)を用いて生きた細胞内部の核の硬さを直接的にナノスケールで計測し、その分布を可視化することに世界で初めて成功しました。
がん細胞の核の硬さは、悪性度や転移能と関係する重要な指標の一つと考えられています。しかし、従来の細胞外からの測定や細胞から取り出した核の測定では、生きた状態の核の硬さを正確に測定することは困難でした。
そこで、本研究では極細の探針を使用することによって生きた細胞内の構造を可視化するナノ内視鏡 AFM 法を応用することにより生きたがん細胞内の核の硬さを直接測定する技術を確立しました。この方法を用いて、がんの転移に関わる「上皮間葉転換(EMT)」(※2)の誘導による影響を測定したところ、EMT が起こると細胞核が柔らかくなることを発見しました 。さらに、この核の硬さの変化は、核膜を裏打ちするラミンタンパク質の発現量とは相関せず、DNA が折りたたまれた構造体であるクロマチン(※3)の凝集度と強く相関していることを突き止めました。
これらの知見は、核の硬さを指標とした新たながん診断技術の開発や、細胞内小器官の力学的な役割の解明につながることが期待されます。
本研究成果は、2025 年 10 月 12 日に国際学術誌『ACS Applied Nano Materials』のオンライン版に掲載されました。
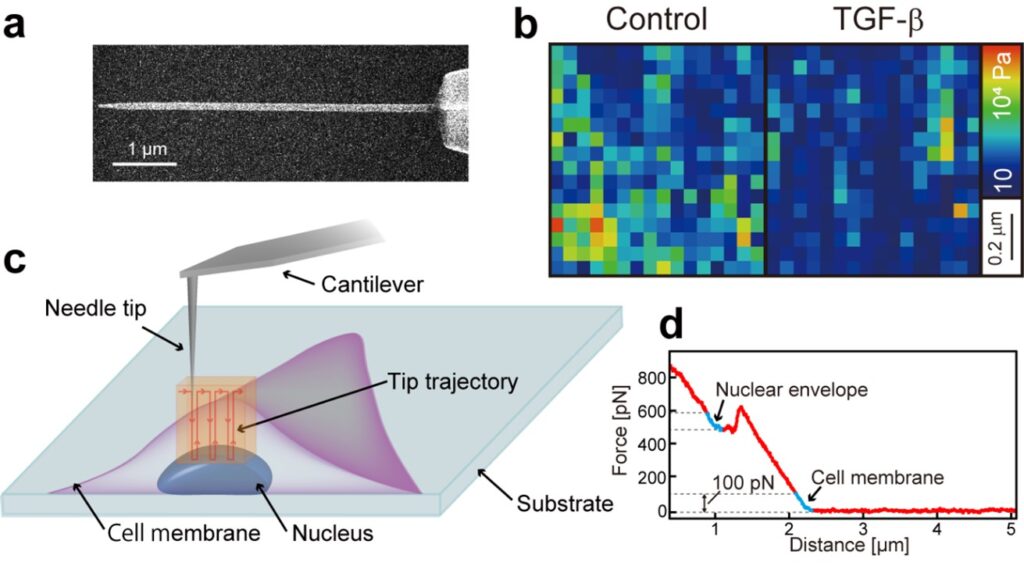
図1:(a)ナノニードル探針の電子顕微鏡写真。(b)核表面の1 mm四方の硬さ分布。(c)ナノニードル探針で生きた細胞の核膜の硬さを測定する模式図。(d)典型的なフォースカーブと細胞膜、核膜に相当する立ち上がり部分。
【用語解説】
※1:原子間力顕微鏡(AFM)
鋭くとがった探針で試料の表面をなぞることで、分子や原子レベルの凹凸像を観察する顕微鏡。探針で試料を押さえつけた際の変形量から、試料の硬さ(弾性率)を計測することも可能。
※2:上皮間葉転換(Epithelial-Mesenchymal Transition, EMT)
細胞同士が強く接着して動けない「上皮細胞」が、接着を失い運動能力の高い「間葉系細胞」の性質を獲得する現象。がん細胞が EMT を起こすことで、原発巣から剥がれ、血管などに侵入して遠隔臓器へ転移する能力を獲得する。
※3:クロマチン
細胞核の中に存在する、DNA とヒストンなどのタンパク質の複合体。DNA をコンパクトに核内に収納する役割を持つ。その凝集度は遺伝子の発現制御に関わっており、固く凝集した「ヘテロクロマチン」と、緩くほどけた「ユークロマチン」に大別される。
..
.
ジャーナル名:ACS Applied Nano Materials







 PAGE TOP
PAGE TOP