金沢大学がん進展制御研究所のニック・バーカー客員教授,寺門侑美博士研究員,村上和弘助教らの国際共同研究グループは,進行したヒト胃がんに非常によく似た胃がんを発症するマウスモデルの樹立に成功しました。また,このモデルを使用した実験により,胃がん組織に存在し,がんの発生と維持,転移に必須である新たな胃がん幹細胞を世界で初めて発見しました。
我が国において,胃がんはその高い罹患率からがんによる死亡原因の第3位です。早期での自覚症状がほとんど無い一方で,進行した胃がんは根治が難しく,主に化学療法が用いられますが,有効な抗腫瘍薬は未だ乏しく新規開発が望まれ続けています。しかし,進行した胃がんに対する効果的な治療法を確立する上で,悪性度の高いヒト胃がんの発生・浸潤・転移を再現できるマウスモデルが存在しないこと,薬剤耐性を示す原因と考えられる胃がん幹細胞 (※1)の詳細が解析されていないことが大きな障害となっていました。
本研究では,胃上皮組織のみで遺伝子変異を誘発できるマウスモデルを開発することで,悪性度の高い胃がんの発生・浸潤・転移を再現できる新たな胃がんマウスモデルの樹立に成功しました。また,その腫瘍組織から樹立した胃がんオルガノイド(※2)を用いた同所移植法を確立し,胃がんの進展を大規模で迅速に解析できる実験系の開発に成功しました。これらの解析系を用いることで,胃がんの発生と維持に必須である新たな胃がん幹細胞を世界で初めて発見しました。そして,これらの胃がん幹細胞を取り除くことで,既存の抗癌剤の効き目が著しく改善することを明らかにしました。
これらの研究成果は,悪性度の高い胃がんの発生・進展・転移過程の詳細な解析を可能にする実験系と胃がん幹細胞に関する新たな知見を提供するものであり,将来的には,進行したヒト胃がんに対する画期的な治療法の開発につながることが期待されます。
本研究成果は,2021年12月2日16時(英国時間)に国際学術誌『Nature Cell Biology』のオンライン版に掲載されました。
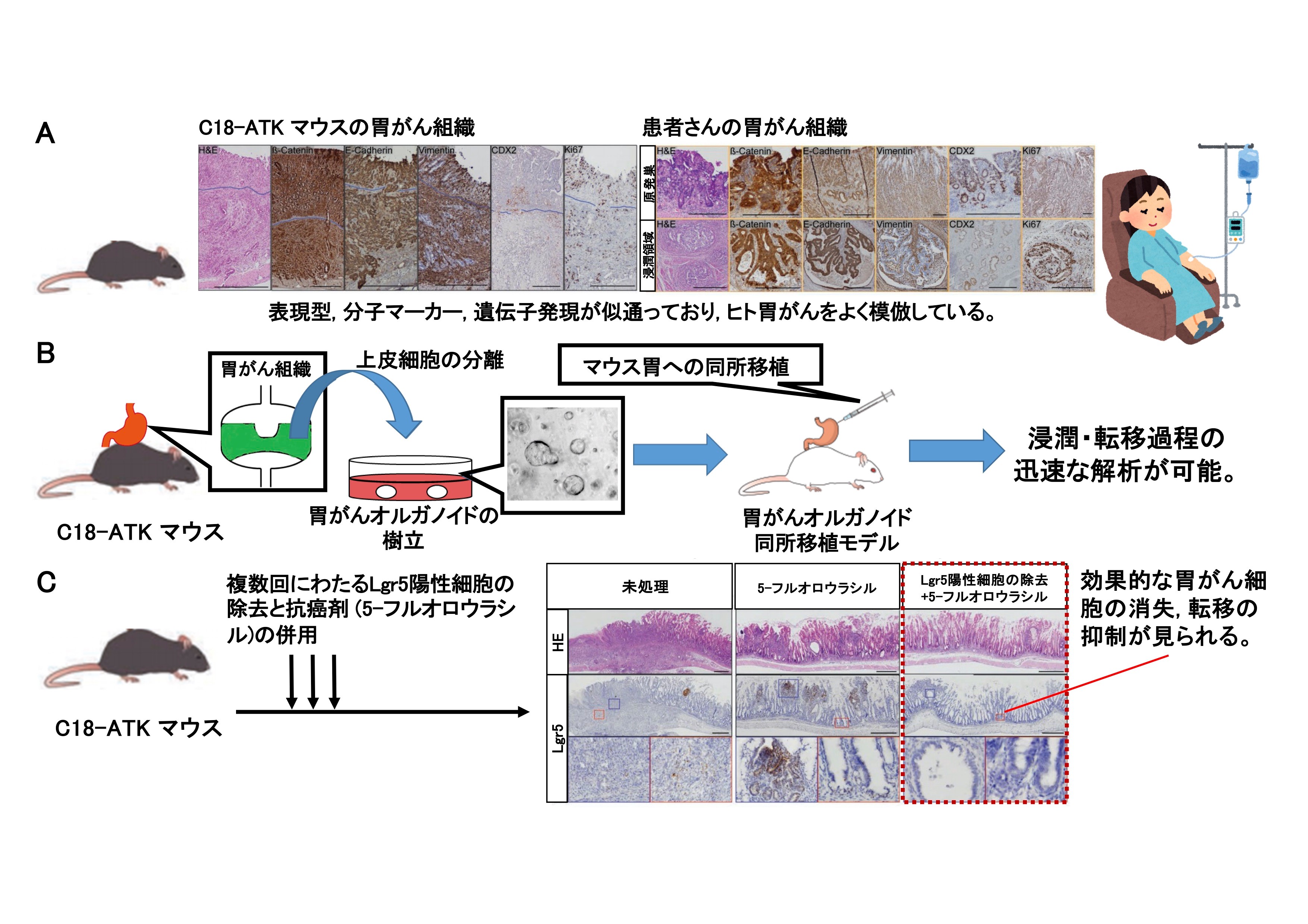
本研究の概要
A.マウス胃上皮選択的に変異を導入するCldn18-IRES-CreERT2ドライバーを開発した。 ヒト胃がんで報告されているWNTとKRAS, TP53変異を組み合わせることで, ヒト転移性胃がんを再現する新規マウスモデル(C18-ATK)の樹立に成功した。ヒトの進行性胃がんを正確に再現することから,胃がん研究のための良いモデルとなり得る。
B.C18-ATKマウスの胃がん組織から樹立した胃がんオルガノイドを用いた同所移植モデルを開発した。この移植モデルを用いることで,解析期間が大幅に短縮でき,質の揃った大規模な解析が可能となる。
C.Lgr5遺伝子(※3)を発現する胃がん幹細胞の除去と既存の抗がん剤の併用により,胃がんの進行が著しく抑制される結果を得た。ヒト胃がんにも存在するLgr5陽性胃がん細胞を標的とすることで,進行した胃がんに対する画期的な治療法が開発できる可能性が示唆された。
【用語解説】
※1 がん幹細胞
自己複製能と多分化能の性質を持っており,抗がん剤による治療を行っても残存し再発を引き起こすがんの親玉のような役割を果たす。
※2 オルガノイド
試験管の中で作ることのできる類臓器。幹細胞のもつ自己複製能・多分化能を利用し3次元的な組織様構造を形成する。従来の2次元培養やスフェロイドとは異なり,生体内の器官に近い特徴を有する。
※3 Lgr5遺伝子
Leucine-rich repeat-containing G-protein coupled receptor 5(Lgr5)はGタンパク質共役受容体であり,Wntシグナルの標的遺伝子として知られている。現在まで,腸管,乳腺,胃,卵巣などさまざまな上皮組織で発現していることが確認されている。とくに,腸管上皮とは密接に関連しており正常腸管上皮のみならず大腸がんの幹細胞マーカーとしても注目されている。




 PAGE TOP
PAGE TOP