金沢大学ナノ生命科学研究所/がん進展制御研究所の大島浩子准教授,大島正伸教授の研究グループは,東京大学の宮園浩平教授,上田泰己教授との共同研究により,遺伝的な多様性を持ったがん細胞集団による転移メカニズムの解明に成功しました。
がん転移機構の新しい概念として,多様性のあるがん細胞集団が細胞塊(クラスター)を形成して体内を移動し,遠隔臓器に転移巣を形成する「ポリクローナル転移(※1)」が提唱されています。しかし,実際に生体内において多様な細胞集団がどのように転移巣を形成するのかは不明でした。本研究グループは,異なるドライバー遺伝子(※2)に変異を持つマウス腸管がん由来のオルガノイド(※3)を用いた移植実験を行い,転移性の高い悪性腸管がん細胞が間質の細胞を活性化させて転移ニッチ(※4)を形成し,これに依存して非転移性がん細胞が混在したポリクローナル転移巣を形成することを明らかにしました。
これらの知見は,従来考えられていた遺伝子変異に依存した転移機構とは異なる,新たながん転移モデルの概念の樹立につながり,新しい大腸がん転移の予防・治療薬の開発に活用されることが期待されます。
本研究成果は2021年2月8日午前10時(英国時間)に 英国科学誌『Nature Communications』のオンライン版に掲載されました。
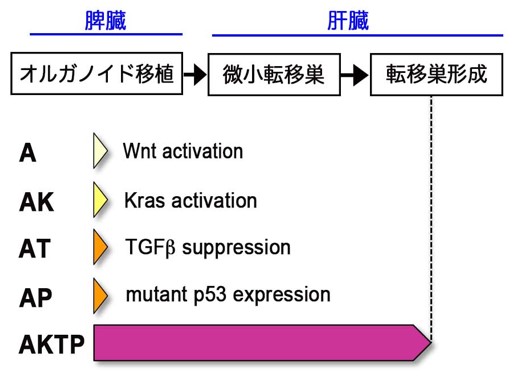
図1. 腸管腫瘍由来オルガノイド(A, AK, AT, AP, AKTP)の説明
各遺伝子変異により誘導される変化(Wnt活性化、Kras活性化等)。AKTP細胞だけが肝転移能を獲得している。
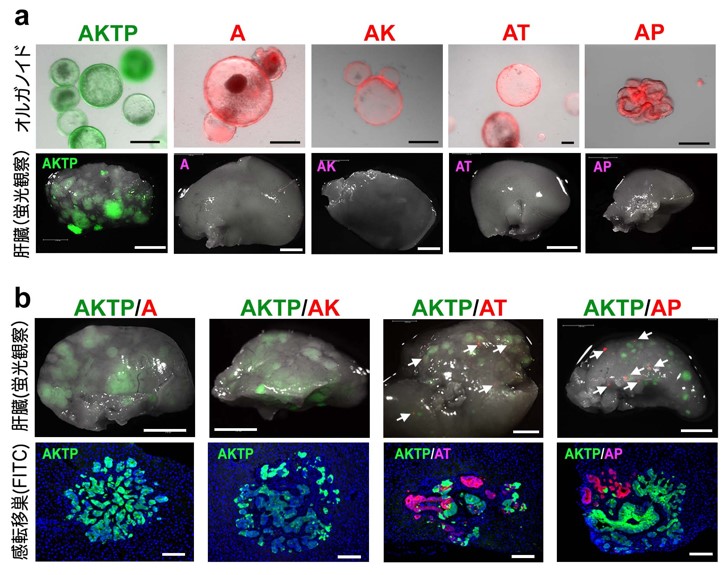
図2. オルガノイド移植実験
(a)蛍光標識した各遺伝子型オルガノイド写真(上段),脾臓移植後の肝臓の蛍光実体顕微鏡写真(下段)。AKTP細胞のみが転移する。
(b)AKTP細胞と非転移性細胞を同時に移植したマウスの肝臓(上段)と蛍光組織染色(下段)。ATとAP細胞はAKTP細胞といっしょに転移巣を形成する。
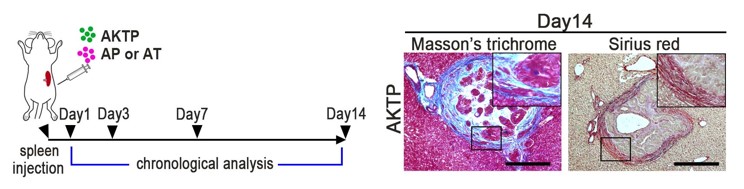
図3. マウスへの細胞移植スケジュール(左)と,AKTP細胞を移植した時に肝臓に形成される転移ニッチ(右:コラーゲン線維染色)
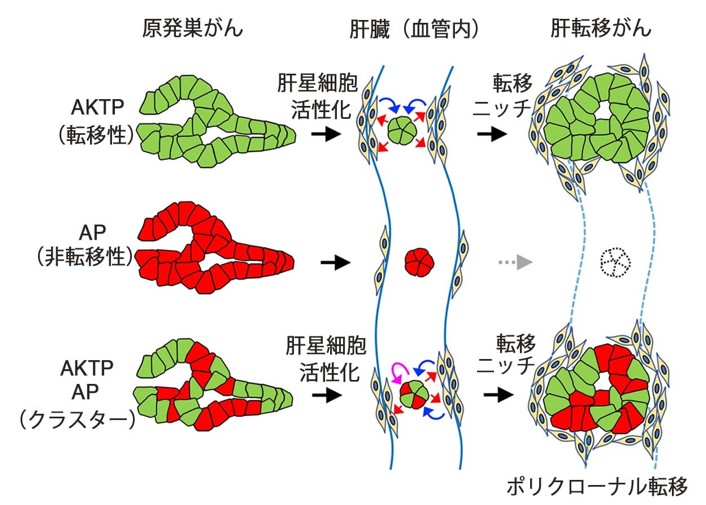
図4. 本研究成果の模式図
転移性がん細胞は肝星細胞を活性化して(赤矢印),転移ニッチを形成し,ニッチの作用により(青矢印)転移巣を形成する。非転移性がん細胞は,転移ニッチの存在や,転移性がん細胞の作用により(ピンク矢印),生存,増殖してポリクローナル転移巣を形成する。
※1 ポリクローナル転移
原発巣で転移能を獲得したがん細胞が単独で転移巣をモノクローナルに形成するという従来の考え方に対して,複数の遺伝的に異なるがん細胞集団がクラスターとして遠隔臓器に血流を介して到達し,多様性を維持したままポリクローナルな転移巣を形成するという仮説。
※2 ドライバー遺伝子
がん細胞で認められる多数の遺伝子変異の中で,その遺伝子の変異が発がんや悪性化,進展に関与する場合,その遺伝子をドライバー遺伝子と呼ぶ。
※3 オルガノイド
正常組織あるいは腫瘍組織由来の上皮細胞を,生体内と同様の腺管等の組織構造を維持したままマトリックス中で3次元培養した組織。生体内の状況に近いと考えられ,これまでの平面状の培養細胞に代わる生体外培養モデルとして広く研究に使われる。
※4 転移ニッチ
がん転移組織で,がん細胞周囲の宿主由来の細胞で形成される微小環境。線維芽細胞,血管内皮細胞,免疫細胞などで構成され,がん細胞の生存や増殖促進に重要な役割を果たす。
研究者情報:大島 浩子
研究者情報:大島 正伸




 PAGE TOP
PAGE TOP