金沢大学医薬保健研究域医学系の西山正章教授,九州大学生体防御医学研究所の中山敬一主幹教授,仁田暁大研究員らの研究グループは,自閉症の原因タンパク質であるCHD8(※1)が,造血幹細胞(※2)の機能維持に重要な役割を果たすことを明らかにしました。
CHD8は自閉症患者において最も高頻度で変異が認められている遺伝子です。CHD8遺伝子に変異を持つ自閉症では,コミュニケーション異常や固執傾向といった自閉症特有の症状が認められます。そのため,神経系に特化した研究が盛んに行われていますが,CHD8は神経系のみならずさまざまな組織で発現しており,特に幹細胞で高発現していますが,その機能はほとんどが不明でした。
本研究グループは,血液細胞に着目して解析すると,造血幹細胞でCHD8の発現量が高いことを突き止めました。そこで,血液細胞におけるCHD8の機能を詳細に解析するため,血液細胞特異的にCHD8を欠損させたマウスを作製して解析しました。その結果,CHD8を欠損した造血幹細胞は,異常な増生が認められるが,幹細胞としての機能は消失していました。この原因を突き止めるために,CHD8欠損造血幹細胞をRNAシークエンス(※3)で網羅的に遺伝子発現状態を評価すると,がん抑制遺伝子のp53(※4)が活性化することで,造血幹細胞から分化した血液細胞を産生する過程で障害を来していることが明らかとなりました。さらに,CHD8とp53を共に欠損させたマウスを作製して解析すると,CHD8欠損により生じた異常が部分的に回復することを突き止めました。
本研究により,自閉症発症の原因遺伝子であるCHD8が造血幹細胞において重要な機能を果たすことが明らかとなり,今後のCHD8遺伝子に変異を持つ自閉症患者の効果的な治療法開発の扶翼となることが期待されます。
本研究成果は,2021年2月2日(火)午前11時(米国東部時間)に米国科学雑誌『Cell Reports』で公開されました。
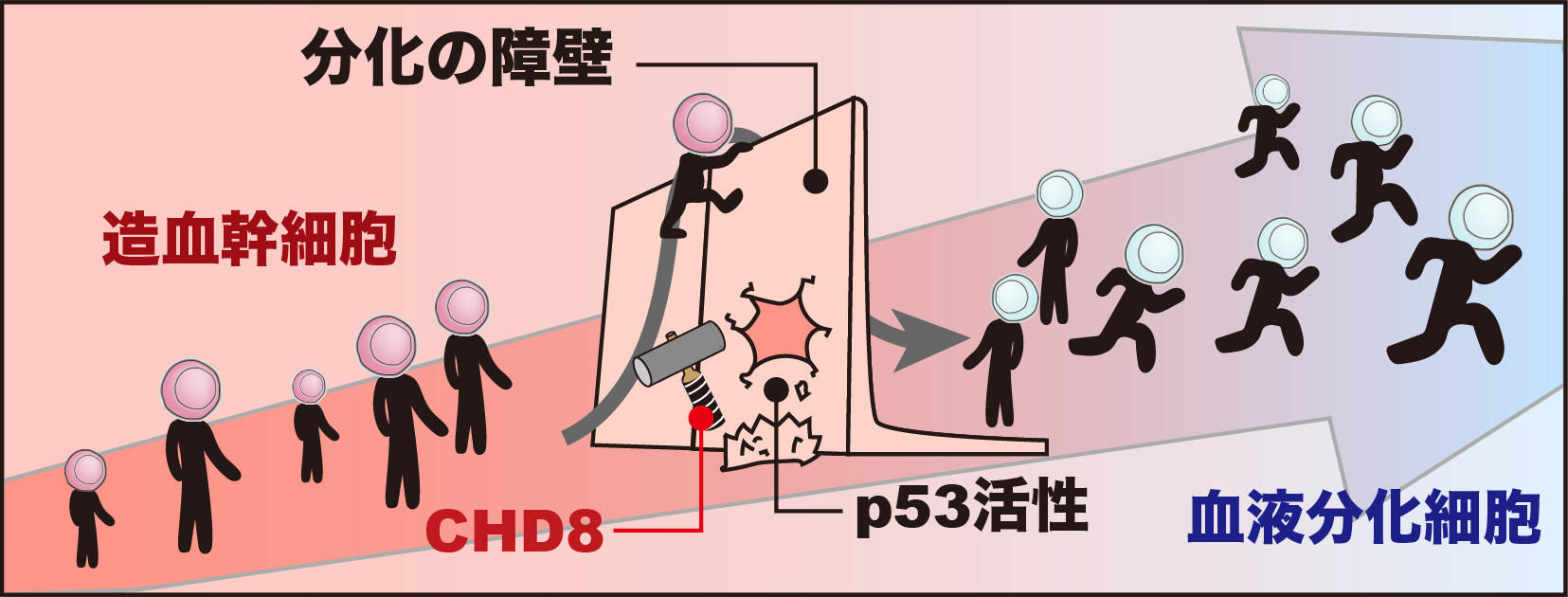
図1. 造血幹細胞から産生される血液分化細胞
造血幹細胞から機能する血液細胞を産生させるためには,がん抑制遺伝子のp53活性による分化の障壁を越える必要があり,CHD8によりp53活性を抑えることで,この障壁を越えることを可能にすることを明らかにしました。
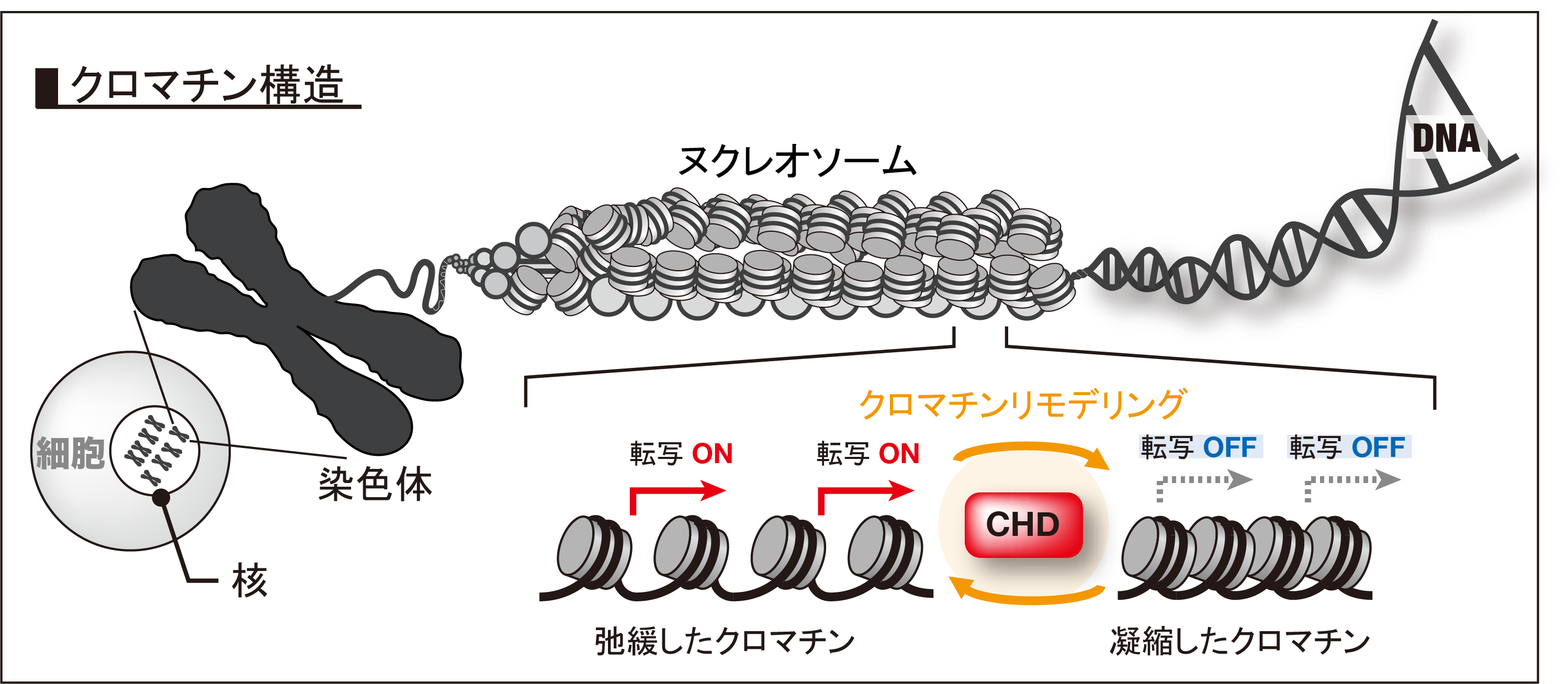
図2. CHD8によるクロマチンリモデリング
染色体(クロマチン)は,DNAがヒストンというタンパク質に巻き付いたヌクレオソームという構造をとることで,高度に折り畳まれて核の中に収納されています。遺伝子が発現する際には,この染色体が弛緩したり凝縮したりすることで制御されています。CHD8はこの染色体の構造を変化させるクロマチンリモデリング活性を有しており,遺伝子の転写のONとOFFを制御しています。

図3. CHD8欠損により造血幹細胞の機能が障害される
造血幹細胞は,骨髄中にごく少数存在しています。正常なマウス造血幹細胞は全骨髄細胞の0.01%存在しますが,CHD8を欠損することでその割合は,およそ0.3%以上と顕著に増加します(左図)。一方で,この増加した造血幹細胞は機能を失っているため,コントロールで認められるコロニーが形成されません(右図)。
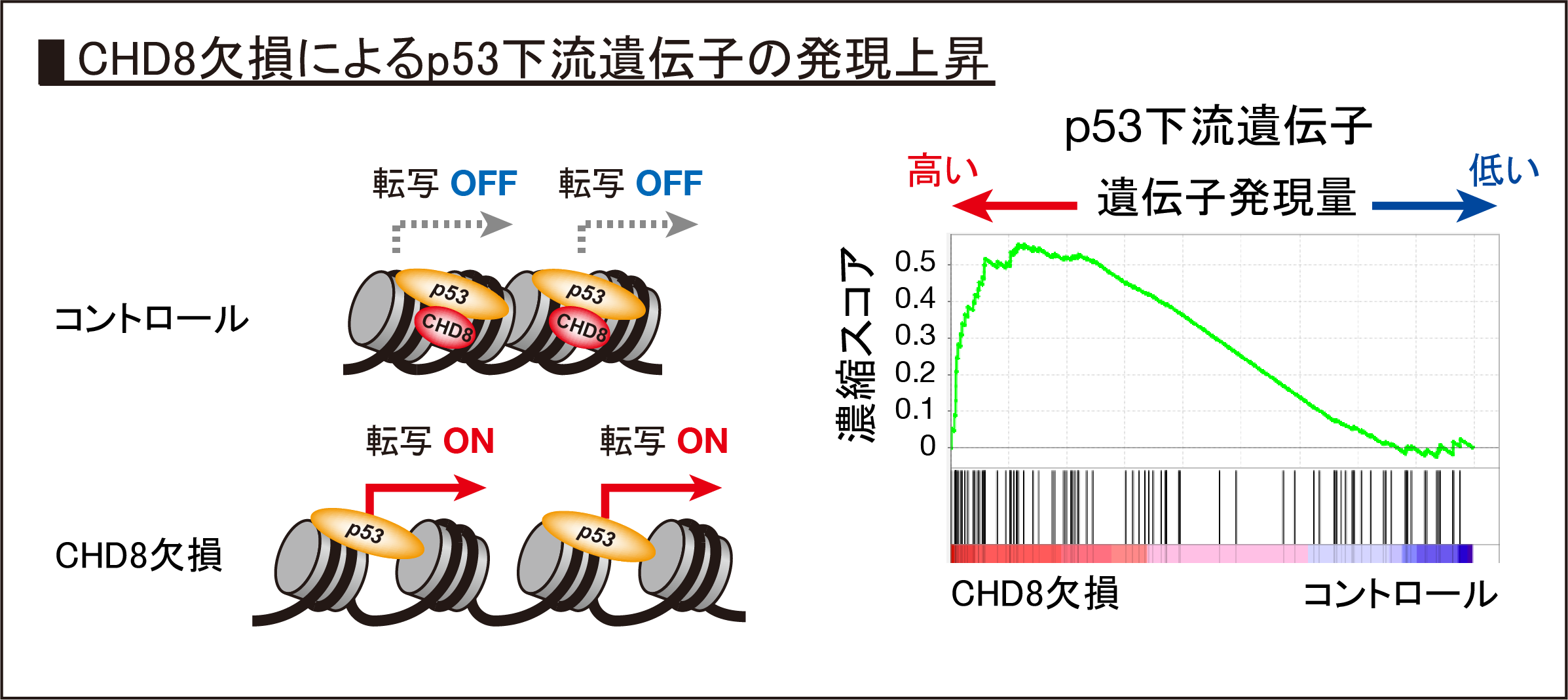
図4. CHD8欠損造血幹細胞ではp53下流遺伝子の発現が上昇している
CHD8はp53遺伝子と結合することでp53下流遺伝子の発現を抑制しています。したがって,CHD8を欠損するとp53が活性化し,p53下流遺伝子の発現が上昇します(左図)。RNAシークエンス解析から,CHD8を欠損した造血幹細胞ではp53下流遺伝子の発現が顕著に増加していることが明らかとなりました。
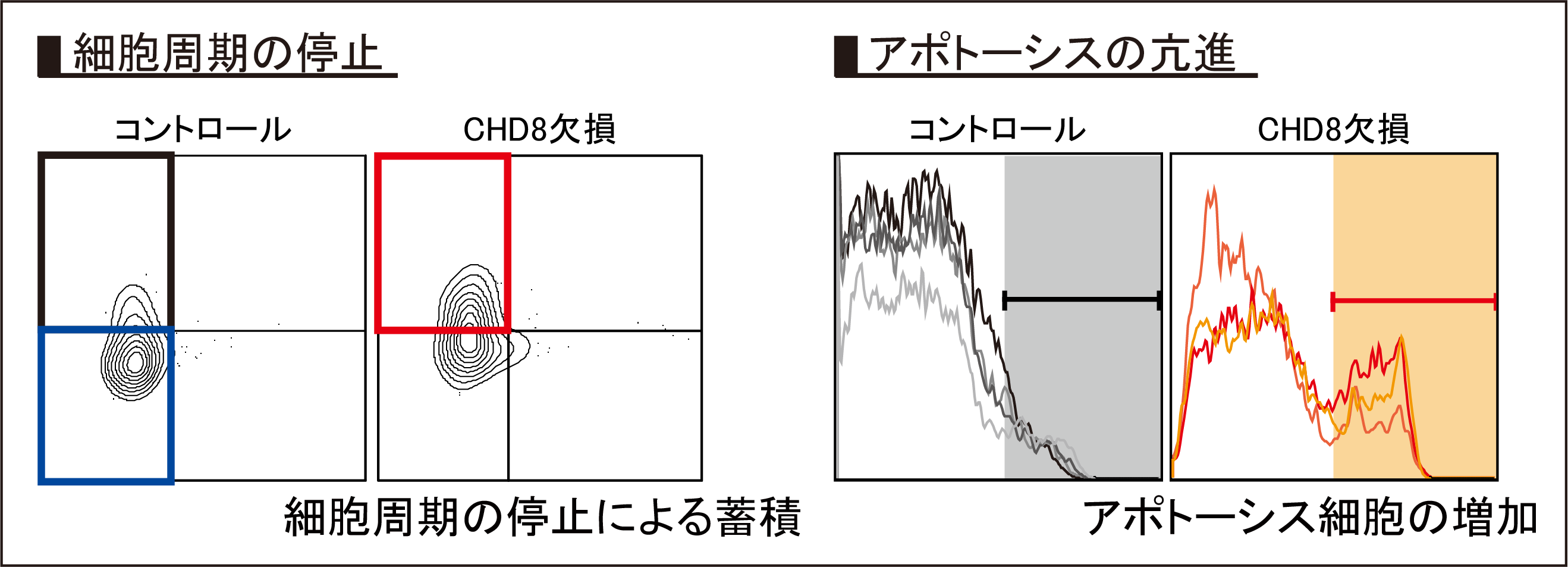
図5. CHD8欠損造血幹細胞は細胞周期が止まりアポトーシスを引き起こす
大半の造血幹細胞は定常状態では細胞周期サイクル回っていませんが(左図の青色枠内),CHD8欠損造血幹細胞では一時的に細胞周期に入るものの(左図の左上枠内),そこで停止してしまうため,次のステップに進めなくなることが分かりました(左図)。さらに,CHD8に欠損によりアポトーシスを引き起こしている細胞の割合がコントロールに比べて顕著に増加していました(右図)。
※1 Chromodomain Helicase DNA binding protein 8 (CHD8)
細胞内のエネルギーを使用して染色体構造を変化させ,遺伝子の発現調節を担うクロマチンリモデリング因子という一群のタンパク質の一種。
※2 造血幹細胞
大人では骨髄中に存在する組織幹細胞の一種。全ての血液細胞に分化する能力を持つ。
※3 RNAシークエンス
細胞から回収したRNAを次世代シークエンサーを用いて大量に読み込むことで,遺伝子の発現量を網羅的に解析する手法。
※4 p53
がん抑制遺伝子の一つで,さまざまな遺伝子の転写を制御することで,細胞増殖や細胞分化,細胞死や細胞老化など多岐に渡って細胞の運命決定を担っているタンパク質の一種。
研究者情報:西山 正章




 PAGE TOP
PAGE TOP