金沢大学医薬保健研究域医学系の伏田幸夫准教授らの研究グループは,肥満細胞から分泌される炎症誘発性低分子タンパク質のインターロイキン-17A(IL-17A)(※1)が,胃がんの腹膜播種における腫瘍組織の線維化(※2)の進行に影響を与えていることを明らかにしました。
胃の粘膜の細胞から発生するがんである胃がんは,徐々に大きくなりながら胃の内側から外側へ向けて進行し,最終的にはおなかの中にがん細胞が散らばる腹膜播種と呼ばれる状態に至ることがあります。一度腹膜播種が起こると,がん細胞が転移した臓器が線維化することで,腸閉塞や閉塞性黄疸を引き起こすだけでなく,抗がん剤や免疫担当細胞がターゲットとする腫瘍にまで届かず,期待した効果が得られないという問題があります。しかしながら,どのようなプロセスで線維化が発生し進行していくのか,そのメカニズムは解明されておらず,その阻止方法も分かっていませんでした。
本研究では,播種巣における線維化が高度になるに従い腫瘍に浸潤している肥満細胞数が増加していることから,肥満細胞が腫瘍の線維化に関係があると推定し調査を実施しました。以前から全身性硬化症やクローン病における臓器の線維化にはIL-17Aが関係していると報告されていたこともあり,播種巣におけるIL-17A産生細胞を調べたところ,肥満細胞そのものであることが分かりました。そこで,腹腔内の臓器を覆っている腹膜中皮細胞にIL-17Aを加えたところ,腹膜中皮細胞は線維芽細胞に形質転換し,コラーゲンなどを分泌することが明らかになりました。さらにマウスの腹腔内に胃がん細胞株とIL-17Aを同時に投与した場合,腹膜播種巣の数やサイズが増大し,腫瘍内の線維化の程度も増強することも証明されました。
本研究の成果は,肥満細胞のIL-17Aの分泌を防ぐことが,播種巣の線維化を防ぐことにつながることを示唆しています。今後は,マウスを用いた線維化を伴う腹膜播種モデルを作成し,肥満細胞の機能を抑制する抗アレルギー薬などの薬剤によって腫瘍の増殖や線維化を制御することで,胃がん腹膜播種の新しい治療法開発につながることが期待されます。
本研究成果は,2020年6月2日に国際学術誌『Gastric Cancer』のオンライン版に掲載されました。
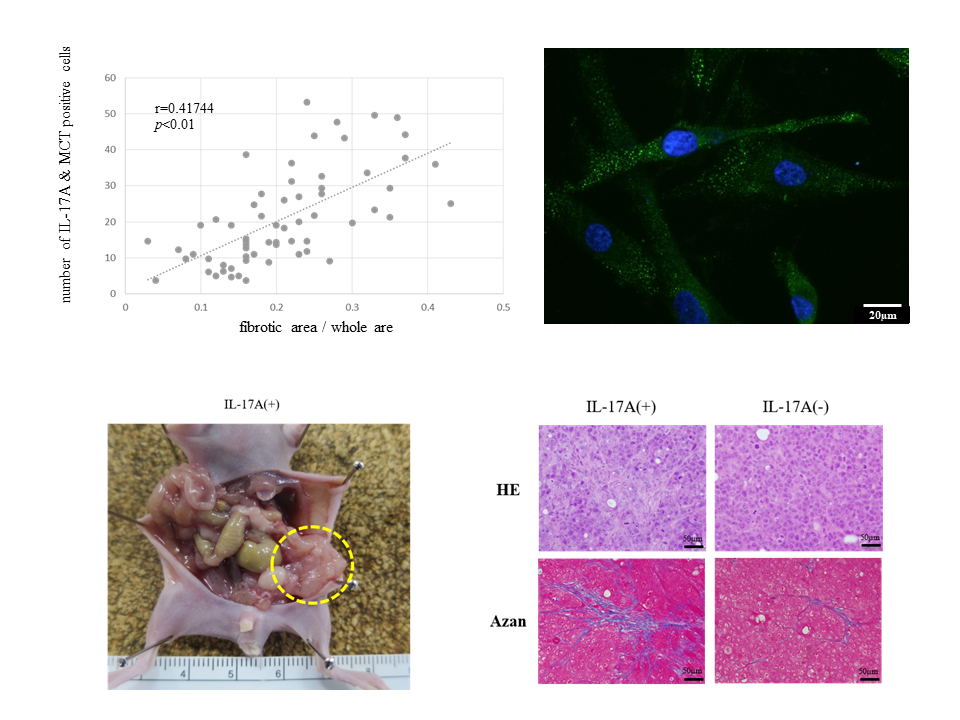
図(左上):腹膜播種巣におけるIL-17A 産生肥満細胞数と腫瘍組織の線維化の程度は正の相関を示した。
図(右上):腹膜中皮細胞にIL-17Aを添加すると紡錘状に形態変化し,がん関連線維芽細胞 (CAF: cancer associated fibroblast)のマーカーであるFAP (fibroblast activating protein)の発現を認めた。
図(左下):高頻度に腹膜播種を形成する胃がん細胞株MKN45-Pを腹腔内投与した後,1,3,7日目にIL-17Aを腹腔内投与すると多数の大きな腹膜腫瘍が形成された。
図(右下):腹膜播種組織における線維化の程度をazan染色で青色に染まる領域の面積で確認すると,IL-17Aを腹腔内投与した群では投与しない群に比較して線維化の程度は高度であることが確認された。
【用語解説】
※1 インターロイキン-17A
主に活性化T細胞 (Th17細胞)から分泌される低分子タンパク質で,線維芽細胞や上皮細胞,血管内皮細胞,マクロファージなどの各種細胞に作用し炎症を誘発させる。
※2 腫瘍組織の線維化
腫瘍組織が線維化を起こすことで,血流は低下し,低酸素環境に陥ったがん細胞は浸潤能を増し抗がん剤耐性となる。
研究者情報:伏田 幸夫




 PAGE TOP
PAGE TOP