金沢大学ナノ生命科学研究所の華山力成教授,河原裕憲助教,医薬保健研究域医学系の中田光俊教授,筒井泰史特任助教の研究グループは,細胞外小胞(※1)による神経膠腫の進展(浸潤・転移)機構の解明に成功しました。
神経膠腫は脳腫瘍の中で最も悪性度が高く,集学的治療を施しても平均生存期間が約2年と非常に予後が悪い腫瘍です。そのため,その進展機構の早急な解明と新規治療法の開発が望まれています。
今回,本研究グループは,腫瘍が分泌する細胞外小胞が,腫瘍関連分子WT1(※2)を腫瘍周囲の細胞へと送達することで新たな血管を作り出し,腫瘍にとって浸潤・転移を起こしやすい環境を構築することを見いだしました。まず,腫瘍細胞をマウス脳内へと移植した脳腫瘍モデルマウスにおいて,腫瘍による細胞外小胞の産生を抑えることで,脳腫瘍サイズが縮小し,浸潤・転移が抑えられ,マウスの生存期間が延長することが分かりました。次に,腫瘍から分泌された細胞外小胞が,腫瘍周囲のミクログリア(※3)に取り込まれ,ミクログリア内の遺伝子発現を調整することで,血管新生を促進することを示しました。さらに,その遺伝子の発現調整因子であるWT1がヒト患者由来の腫瘍由来細胞外小胞に含有されており,ミクログリアによる血管新生能を制御することを明らかにしました。
本研究により,神経膠腫の進展に細胞外小胞が深く関与しており,その産生を抑えることで,腫瘍の浸潤・転移を抑えることができる可能性が示されました。今後,神経膠腫の早期発見や予後診断,新たな治療法の開発へと研究が発展することが期待されます。
本研究成果は,2020年5月28日に英国科学誌『Carcinogenesis』に掲載されました。
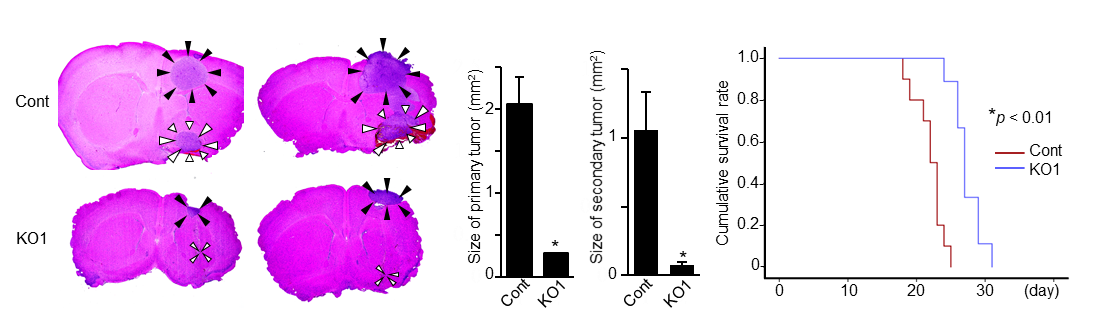
図1. 細胞外小胞の産生と神経膠腫の浸潤・転移能との関連性
細胞外小胞の産生を低下させた神経膠腫細胞株(KO1)を樹立し,対照細胞株(Cont)と進展能の比較を行った。KO1を脳内に移植したマウスでは,腫瘍サイズの縮小(左)と浸潤・転移能の低下(中)が観察され,マウスの生存期間にも有意な差を認めた(右)。
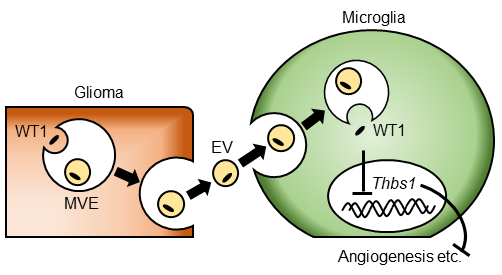
図2. 細胞外小胞による血管新生制御のモデル図
神経膠腫(Glioma)内の多胞性エンドソーム(MVE)の中で細胞外小胞(EV)が形成される際に WT1が含有される。腫瘍から分泌され,ミクログリア(Microglia)に取り込まれたEVは,その内部でWT1を放出し,血管新生を阻害するトロンボスポンジン(Thbs1)(※4)の遺伝子発現を低下させる。その結果,ミクログリアによる血管新生(Angiogenesis)が増強され,腫瘍の浸潤・転移を促進する。
【用語解説】
※1 細胞外小胞
細胞が分泌する脂質二重膜に覆われた小胞のこと。分泌細胞由来のタンパク質やRNAなどの核酸,脂質などを含んでおり,さまざまな細胞間情報伝達を担っている。
※2 WT1
Wilm’s tumor-1遺伝子からつくられるタンパク質。小児腎臓腫瘍の原因遺伝子として発見されたが,白血病や肺がんなど,多くの腫瘍細胞に発現している。
※3 ミクログリア
中枢神経系における免疫細胞の一種。免疫のみならず,腫瘍の増大や浸潤,血管新生,薬剤抵抗性などにも関与することが知られている。
※4 トロンボスポンジン
細胞の移動・接着・増殖などさまざまな機能に関与するタンパク質。血管新生を阻害する。
研究者情報:華山 力成
研究者情報:河原 裕憲
研究者情報:中田 光俊
研究者情報:筒井 泰史




 PAGE TOP
PAGE TOP