金沢大学ナノ生命科学研究所の前田勝浩教授,廣瀬大祐博士研究員,大学院自然科学研究科物質化学専攻博士前期課程2年 (研究当時)の磯部朝日さん,サンティアゴ・デ・コンポステーラ大学のフェリックス フレイレ 博士らの国際共同研究グループは,鏡像異性体(エナンチオマー)(※1)を分離する能力である光学分割能を異なる3つの状態に自在に切り替え可能な革新的な高速液体クロマトグラフィー(HPLC)(※2)用のキラル固定相(※3)を開発しました。
キラル化合物の鏡像異性体は,その物理的・化学的性質がほとんど同じであるため,一般に分離するのが非常に難しい物質です。しかし,鏡像異性体間で生体に対する効果が全く異なることから,特に医薬・農薬などの生理活性物質の開発において,鏡像異性体の分離・分析は欠かすことができません。キラル固定相を用いたHPLCによる鏡像異性体の分離は,分析と分取の両方に有効な方法であり,これまでにさまざまなキラル固定相が開発されてきました。しかし,既存のキラル固定相では分離・分析が困難なキラル化合物が未だ多く存在しているため,新しいタイプのキラル固定相を開発することは非常に重要な課題となっています。
本研究グループは,溶液中で金属イオンに応答してその巻き方向が変化するらせん高分子が,固体状態でも金属イオンを含む溶液で処理することによってらせんの巻き方向を3つの状態(右巻き,左巻き,右巻きと左巻きの等量混合状態)に制御できることを見いだしました。さらに,このポリマーをシリカゲルにコーティングしてHPLC用のキラル固定相として応用し,ナトリウムイオン(Na+)もしくはセシウムイオン(Cs+)を含む溶離液をカラム内に通液する前処理でらせんの巻き方向を制御することによって,異なる光学分割能を示す3つの状態に自在に切り替えが可能なキラル固定相として機能することを実証しました。この新しい固定相は,従来のキラル固定相とは全く異なり,同じキラル固定相を利用して標的物質に応じて最適な光学分割能を示す状態を選択できるだけでなく,鏡像異性体の溶出順序を反転することも可能になります。
本研究成果は,光学分割能を多段階に切り替え可能なキラル固定相を開発するための新しい戦略を提供したといえ,医薬品等の研究開発などキラル化合物を扱うあらゆる分野の発展につながることが期待されます。
本研究成果は,2019年5月7日(米国東海岸標準時間)にアメリカ化学会誌『Journal of the American Chemical Society』のオンライン版に掲載されました。
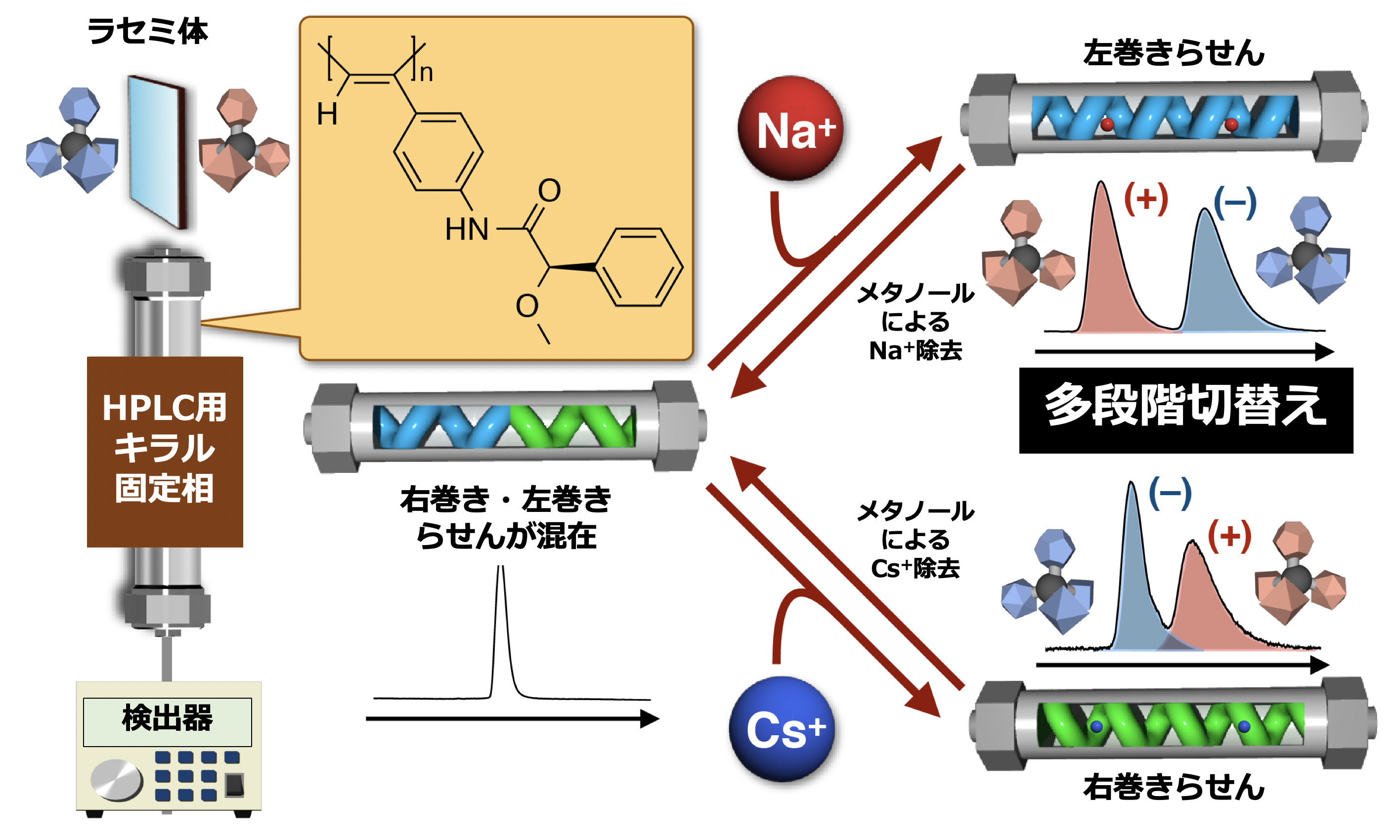
図.
ナトリウムイオン(Na+)やセシウムイオン(Cs+)の添加および除去により固体状態でらせんの巻き方向(右巻き,左巻き,右巻きと左巻きの等量混合状態)が変化するらせん高分子は,異なる光学分割能を示す3状態に自在に切り替えが可能なHPLC用キラル固定相として機能する。最適な光学分割能を示す状態を選択できるだけでなく,鏡像異性体の溶出順序を反転(スイッチ)することも可能になる。
【用語解説】
※1 鏡像異性体(エナンチオマー)
互いに鏡写しの関係にある分子であり,右手と左手の関係のように互いに重ね合わせることができない。このような性質をキラリティといい,この性質を持つキラル分子は医薬・農薬などの生理活性物質中にも多くみられるが,ほとんどの物理的・化学的性質が同じであるため分離が困難である。しかし,生体はその違いを強く認識するため,有用な鏡像異性体のみを得るための分離・分析技術の開発が進められている。
※2 高速液体クロマトグラフィー(HPLC: High Performance Liquid Chromatography)
移動相溶媒を加圧し高速で混合物を分離・分析する手法。試料を カラムと呼ばれる固定相が充填された管の中を通すことで,固定相と化合物の吸着の差異に基づく溶出時間の差を利用した分離を行う。
※3 固定相
HPLCのカラムの中の充填物であり,固定相と化合物の吸着の差異などを利用して各成分の溶出時間に差を生み出す。中でもキラル分子を固定相とするものはキラル固定相と呼ばれ,一般的な固定相では分離することができないキラル分子の鏡像異性体の分離を可能にする。
Journal of the American Chemical Society
研究者情報:前田 勝浩




 PAGE TOP
PAGE TOP