金沢大学医薬保健研究域保健学系の本多政夫教授および村居和寿博士研究員らの研究グループは,医薬保健研究域医学系の金子周一教授および篁俊成教授らとともに,C型肝炎ウイルス(HCV : Hepatitis C virus)(※1)感染時に, 主に肝臓で産生される分泌タンパク質であるセレノプロテインP(※2)のmRNAが,抗ウイルス免疫分子であるRIG-I(Retinoic acid-inducible gene-I)(※3)と結合することで,その機能を阻害し,自然免疫機構を制御することを明らかにしました。
C型肝炎に感染すると,同時に,インスリンの機能低下による代謝異常を特徴とする2型糖尿病になりやすいことが知られています。また,C型肝炎の治療には抗ウイルス薬の投与などを使用する治療が中心となりますが,2型糖尿病を患ったC型肝炎患者では,インターフェロン(IFN)による抗ウイルス治療の効果が低いことが報告されていました。しかし,そのメカニズムや因果関係は未だ明らかにはされていませんでした。
今回,本研究グループは,世界に先駆けて報告したセレノプロテインPというインスリン抵抗性を引き起こし,2型糖尿病の病態形成に関与するタンパクに着目し,培養細胞・マウス・臨床検体を用いた研究によって,HCV感染・自然免疫・代謝性疾患の関係性を明らかにしました。HCV感染によって発現誘導されたセレノプロテインPのmRNAが,抗ウイルス免疫分子であるRIG-Iタンパクに結合し,活性化に必要な構造変化を妨げることにより,抗ウイルス作用を有するIFNの誘導を抑制していることが分かりました。
これらの知見は将来,ウイルス感染や代謝性疾患による免疫システム破綻のメカニズムの解明に活用されることが期待されます。
本研究成果は,2019年4月10日午前11時(米国東海岸標準時間)米国科学誌『Cell Host & Microbe』のオンライン版に掲載されました。
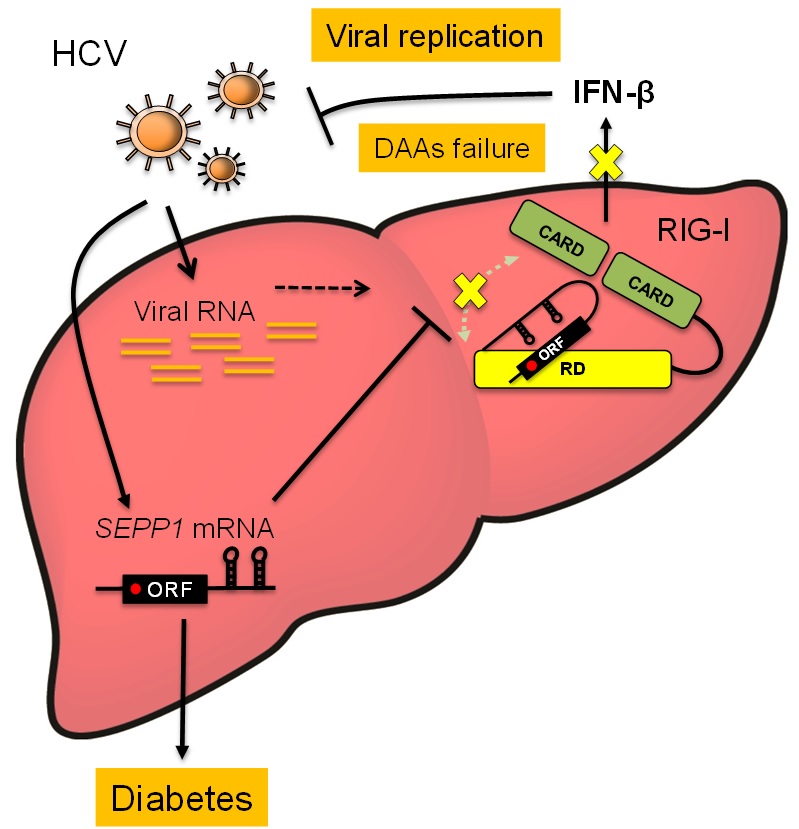
図. HCV感染によって誘導されたセレノプロテインPのmRNAによる自然免疫制御メカニズム
HCVが感染した肝臓において,セレノプロテインP(SEPP1)の発現上昇が起こる。セレノプロテインPのタンパクはインスリン抵抗性を惹起し,2型糖尿病(Diabetes)の病態形成を促進する。
一方,セレノプロテインPがコードされている遺伝子であるセレノプロテインPのmRNAは,RIG-Iの制御ドメイン(Regulatory domain:RD)に結合し,抗ウイルス作用を有するI型インターフェロン(IFN-β)の産生を阻害する。その結果,ウイルス複製(Viral replication)が上昇しDAAs療法に抵抗性を示すようになる。
※1 C型肝炎ウイルス(HCV : Hepatitis C virus)
フラビウイルス科ヘパシウイルス属に属するRNAウイルスで,C型肝炎の原因となる。
※2 セレノプロテインP
必須微量元素であるセレン(Se)の輸送タンパクであり,主に肝臓で産生される分泌タンパク質である。
※3 RIG-I(Retinoic acid-inducible gene-I)
自然免疫系で働くタンパク質の分子であり,ウイルスが細胞内に進入した時にウイルス由来のRNAを認識し,抗ウイルス作用を示すI型インターフェロン産生の誘導を引き起こす。
・ 詳しくはこちら
・ 研究者情報:本多 政夫
・ 研究者情報:金子 周一
・ 研究者情報:篁 俊成




 PAGE TOP
PAGE TOP